Schedule a Visit
Nulla vehicula fermentum nulla, a lobortis nisl vestibulum vel. Phasellus eget velit at.
Call us:
1-800-123-4567
Send an email:
monica.wayne@example.com
Nulla vehicula fermentum nulla, a lobortis nisl vestibulum vel. Phasellus eget velit at.
Call us:
1-800-123-4567
Send an email:
monica.wayne@example.com
Margit Fisch – Gianluca D’Elia – Rudolf Hohenfellner
Nel 1952 Uebelhor descrisse per primo una derivazione urinaria utilizzando un segmento escluso del grosso intestino (1). Tale tecnica offriva il vantaggio di una anastomosi ureterale antireflusso ed allo stesso tempo un minimo rischio di stenosi dello stoma o di un allungamento sproporzionato dell’ansa esclusa in rapporto alla crescita corporea (2, 3, 4). Le derivazioni urinarie continenti in seguito soppiantarono il condotto colico. Oggigiorno esso sembra invece aver riacquistato importanza almeno come forma “temporanea” di derivazione urinaria (5, 6). Situazioni cllniche imprevedibili, come ureteri dilatati e/o compromissione della funzione renale, necessitano temporaneamente di una derivazione urinaria a pressione nulla (vedi il caso dei pazienti con meningomielocele). Dopo regressione della dilatazione e stabilizzazione della funzione renale si può eventualmente incorporare il condotto sigmoideo in una delle varie forme di derivazione continente attualmente disponibili (7, 8) (vedi capitolo 9.2 – Conversione urinaria).



– Derivazione urinaria incontinente in età pediatrica. – Derivazione urinaria temporanea con opzione futura per una conversione in una derivazione continente.
– Laparotomia mediana. – Incisione paracolica sinistra. – Scelta del segmento sigmoideo (12-15 cm) facendo attenzione a preservarne la vascolarizzazione. – Esclusione del segmento sigmoideo dalla continuità intestinale. – Identificazione, preparazione e sezione degli ureteri al loro ingresso in vescica. – Il reimpianto ureterale antireflusso può essere eseguito sia in tecnica “open-end” (vedi capitolo 8.5 – Condotto colico-trasverso) sia in tecnica transcolonica dopo apertura longitudinale del segmento escluso (“button-hole”). – In quest’ultimo caso si procede alla chiusura dell’estremità craniale del condotto con punti staccati sieromuscolari. – Apertura antimesenteriale del condotto per una lunghezza di ca. 4 cm a livello della tenia libera ed in prossimità della sua estremità craniale. – Incisione della parete sigmoidea esterna posteriore per creare un canale per il passaggio ureterale. – Preparazione del tunnel sottomucoso di una lunghezza di ca. 3-4 cm. – Punto di ancoraggio alle ore 6 tra uretere e sieromuscolare colica (catgut cromico 5/0). – Anastomosi muco-mucosa uretero-intestinale (catgut cromico 6/0). – Posizionamento di tutori ureterali 6 Charr, che vengono fatti fuoriuscire dall’estremità aborale del condotto. – Ripristino della continuità intestinale tramite anastomosi termine-terminale colo- colica con punti staccati riassorbibili sieromuscolari. – Chiusura dell’incisione longitudinale antimesenteriale colica con punti sieromuscolari staccati. – Creazione dello stoma tramite incisione circolare della cute ed incisione a forma di croce della fascia e del peritoneo. – Si fissa l’estremità aborale del condotto alla fascia ed alla cute con formazione definitiva dello stoma.
– L’esclusione del segmento sigmoideo dalla continuità intestinale va eseguita facendo attenzione a preservare la vascolarizzazione di questo tratto intestinale (rami sigmoidei dell’arteria mesenterica inferiore). Di regola, ad una distanza di circa 6 cm distalmente e prossimalmente al ramo principale si può individuare una posizione ideale ove incidere il mesentere e preservare in modo ottimale la vascolarizzazione del condotto. Il segmento escluso in questa posizione è di solito molto mobile. – L’uretere destro viene reimpiantato ad una distanza di ca. 3 cm dal sinistro ed in posizione leggermente prossimale rispetto a quest’ultimo. – In sede di chiusura dell’incisione mesenteriale si può ottenere una extraperitonealizzazione dell’estremità craniale del condotto, che includa anche l’anastomosi uretero-intestinale. Una volta creato lo stoma si può fissare il condotto alla parete addominale laterale ottenendo così la extraperitonealizzazione di tutto il condotto.
1. Uebelhoer R. Die Darmblase. Langenbecks Arch Klin Chir 1952; 271: 202.2. Hohenfellner R, Wulff HD. Zur Harnableitung mittels ausgeschalteter Darmsegmente. Akt Urol 1970; 1: 18.3. Skinner DG, Gottesmann JE, Richie JP. The isolated sigmoid segment: its value in temporary urinary diversion and reconstruction. J Urol 1975; 113: 614.4. Hendren WH. Exstrophy of the bladder. An alternative method of management. J Urol 1975; 115: 195.5. Hendren WH. Non-refluxing colon conduit for temporary or permanent urinary diversion in children. J Pediatr Surg 1975; 10: 381.6. Morales P, Golimbu M. Colonic urinary diversion. 10 years of experience. J Urol 1975; 113: 302.7. Stein R, Fisch M, Stoeckle M, Demirkesen O, Hohenfellner R. Colonic conduit in children: protection of the upper urinary tract 16 years later ? J Urol 1996; 156: 1146.8. Wammack R, Fisch M, Hohenfellner R. Conversion and undiversion surgery. Urologia 1993; 60: 127.
Margit Fisch – Gianluca D’Elia – Rudolf Hohenfellner
A partire dalla prima pubblicazione nel 1967, l’utilizzazione del colon trasverso ai fini della creazione di una derivazione urinaria in pazienti affetti da neoplasie maligne ginecologiche o urologiche sottoposti a radioterapia è andata progressivamente affermandosi (1, 2, 3). Infatti, in relazione alla sua localizzazione nell’emiaddome superiore, il colon trasverso rappresenta un segmento intestinale escluso dalle lesioni attiniche croniche conseguenti ad una terapia radiante pelvica (4, 5). Inoltre, in considerazione della presenza di un ampio e mobile mesocolon, il colon trasverso ha la versatilità di potersi adattare alle esigenze anatomiche individuali della situazione operatoria. La possibilità di effettuare un impianto ureterale antireflusso in un tunnel sottomucoso rappresenta un ulteriore vantaggio dell’uso del colon trasverso per la derivazione urinaria. Infine, la frequenza di stenosi dello stoma cutaneo è decisamente inferiore rispetto a quelle descritte per il condotto ileale. La decisione se confezionare un condotto colico-trasverso o una tasca colica continente (vedi capitolo 8.7 – Tasca colica) dipende dalle condizioni generali e dall’aspettativa di vita del paziente.











– Pazienti che necessitano di una derivazione urinaria, precedentemente irradiati per neoplasia ginecologica o urologica. – Incontinenza a seguito di cistite attinica. – Fistole vescico-vaginali o vescico-vagino-intestinali dopo radioterapia pelvica. – Patologie a carico di altri segmenti dell’intestino crasso che ne impediscono l’utilizzazione per una derivazione urinaria.
– Laparotomia mediana xifo-pubica con incisione che circonda l’ombelico. – Identificazione degli ureteri a livello dei vasi iliaci. – Isolamento degli ureteri prossimali, fino al di sopra del campo irradiato, al fine di ottenere dei monconi ureterali con adeguata vascolarizzazione e peristalsi. Sezione degli ureteri. – Isolamento del colon trasverso tramite separazione dal grande omento, sezione del legamento gastro-colico, apertura della retrocavità degli epiploon ed, eventualmente, ampia mobilizzazione di entrambe le flessure coliche. – Previa incisione mesenteriale, si procede all’esclusione dalla continuità intestinale di un segmento di colon trasverso di ca. 10-15 cm, preservandone la vascolarizzazione. A questo scopo è utile l’identificazione del decorso dei vasi in controluce. – Ripristino della continuità intestinale tramite anastomosi termino-terminale colo- colica con sutura sieromuscolare in singolo strato a punti staccati in PDS 4/0. – Chiusura della breccia mesenterica con sutura in continua. – Lavaggio del segmento intestinale escluso. – Il colon trasverso può essere anastomizzato alla cute sia in senso peristaltico sia in senso antiperistaltico (6). Lo stoma può perciò venire a trovarsi sia nella metà destra sia in quella sinistra dell’addome. A seconda della posizione dello stoma si dovrà passare l’uretere sinistro o quello destro dietro la radice mesenteriale. REIMPIANTO URETERALE ANTI REFLUSSO CON TECNICA “OPEN END” (7) – Apertura parziale del condotto lungo la tenia libera per ca. 4 cm partendo dall’estremità scelta per l’impianto ureterale. – Accostamento degli ureteri al margine del colon trasverso inciso. – Posizionamento di punti di trazione e preparazione di un tunnel sottomucoso per ciascuno dei due ureteri a partire dal margine prossimale del condotto. La lunghezza del tunnel è di ca. 3-4 cm. – Controincisione della mucosa colica all’estremità opposta del tunnel. – Introduzione degli ureteri nel tunnel sottomucoso, spatulamento degli ureteri ed accorciamento degli stessi, corrispondente alla lunghezza del tunnel. – Posizionamento di due punti di ancoraggio alle ore 5 e 7 tra la parete ureterale e la sieromuscolare intestinale. – Adattamento muco-mucoso uretero-intestinale a punti staccati. – Posizionamento di splint ureterali 6 Charr, fissati alla parete intestinale con catgut 4/0. – Gli splint vengono fatti fuoriuscire dall’estremità aborale del condotto che è quella che si abboccherà alla cute. – Chiusura dell’estremità orale del condotto tramite un singolo strato a punti staccati. – Per prevenire una dislocazione si procede a fissare il condotto al retroperitoneo. REIMPIANTO URETERALE REFLUENTE SECONDO WALLACE (8) – Si spandano gli ureteri per ca. 3 cm e si cateterizzano con degli splint. – Punto di trazione a livello dell’estremità prossimale dell’incisione degli ureteri fatto passare attraverso entrambi gli ureteri, che vengono così accostati. – Anastomosi in continua del margine mediale degli ureteri. Si forma così un “piatto” ureterale. – Fissazione degli splint alla parete intestinale con catgut 4/0 e passaggio degli stessi attraverso il condotto. – Anastomosi tra piatto ureterale precedentemente formato ed estremità libera del colon trasverso (di solito estremità orale) a punti staccati o in continua. CONFEZIONE DELLO STOMA – Incisione circolare della cute. – Incisione a croce della fascia. – Isolamento del condotto dal grasso e dalle appendici epiploiche alla sua estremità aborale. – Passaggio verso l’esterno degli splint attraverso lo stoma così creato. – Si fissa la sieromuscolare intestinale tramite punti staccati alla fascia. – Si adatta quindi la mucosa colica alla cute con punti staccati.
In pazienti con ureteri severamente danneggiati dalla radioterapia, o in caso di fibrosi retroperitoneale con coinvolgimento del terzo prossimale degli ureteri fino entro l’ilo renale, o ancora in casi di tumori uroteliali recidivanti in paziente monorene, è possibile eseguire una anastomosi direttamente tra colon trasverso e pelvi renale (9). Ciò è facilitato dagli stretti rapporti di contiguità che il colon trasverso contrae con la pelvi renale. Per eseguire una pielo-trasverso-cutaneostomia è necessaria una estesa mobilizzazione intestinale (vedi capitolo 7.1 – Vie di accesso al retroperitoneo). Ciò è necessario a causa della posizione alta del condotto trasverso che verrà a trovarsi subito di fronte alla porzione ascendente del duodeno con il pericolo di una sua compressione. Dopo aver posizionato le anse del tenue sul torace del paziente si procede ad isolare gli ureteri fino al giunto pielo-ureterale, ove avviene la sezione ureterale. Si effettua poi la spatulazione di un lungo tratto della pelvi renale. L’anastomosi uretero-pielica destra è termine-terminale mentre quella sinistra è latero- terminale con l’estremità aborale del trasverso che viene poi abboccata alla cute. In casi particolari si può posizionare lo stoma a destra effettuando anastomosi inverse.
1) Mogg RA. Urinary diversion using the colonic conduit. Br J Urol 1967; 39: 687.2) Morales P, Golimbu M. Colonic urinary diversion. 10 years of experience. J Urol 1975;113: 302.3) Altwein JE, Hohenfellner R. Use of the colon as a conduit for urinary diversion. Surg Gynecol Obstet 1975; 140: 33.4) Schmidt JD, Buchsbaum HJ, Jacobo EC. Transverse colon conduit for supravesical urinary tract diversion. Urology 1976; 6: 543.5) Schmidt JD, Buchsbaum HJ, Nachtsheim DA. Further experience with and modifications of the transverse colon conduit in urinary tract diversion. Br J Urol 1985; 57: 284.6) Leadbetter WF, Clarke BG. Five years experience with ureteroenterostomy by the “combined” technique. J Urol 1954; 73: 67.7) Hohenfellner R, Wulff HD. Zur Harnableitung mittels ausgeschalteter Darmsegmente. Akt Urol 1970; 1: 18.8) Wallace DM. Ureteric diversion using a conduit: a simplified technique. Br J Urol 1966; 38: 522.9) Lindell O, Lehtonen T. Rezidivierende urotheliale Tumoren in Einzelnieren mit Anschluss eines Kolonsegmentes an das Nierenbecken. Akt Urol 1988; 19: 130.
Rudolf Hohenfellner – Joachim W. Thueroff
Nel 1983 è stato utilizzato per la prima volta un segmento ileo-cecale detubularizzato e riconfigurato in forma di Mainz Pouch I per eseguire un ampliamento di vescica in un paziente con vescica tubercolotica (MAINZ = Mixed Augmentation Ileum ‘N Zecum) (1). Il razionale di incorporare il colon al serbatoio urinario era quello di permettere un impianto ureterale antireflusso usando la tecnica del tunnel sottomucoso. In seguito, la Mainz Pouch 1 fu utilizzata per la sostituzione vescicale eseguendo un’anastomosi tra il punto più declive del polo recale (o, in alternativa, moncone di 0,5 cm di appendice vermiforme) ed uretra membranosa. L’indicazione ad eseguire una neovescica ortotopica, nonostante si sia estesa negli ultimi anni, deve sempre essere analizzata criticamente, in particolare in presenza di neoplasie avanzate, di carcinomi multifocali o coinvolgenti il collo vescicale e di carcinoma in situ. Controindicazione assoluta è rappresentata dalla presenza di biopsie positive a livello dell’uretra prostatica, caso in cui va eseguita una uretrectomia primaria in sede di cistoprostatectomia radicale. In questi casi, ed in pazienti con patologia benigna in cui la minzione spontanea trans- uretrale sia impossibile o difficoltosa con necessità di cateterismo intermittente (pazienti con vescica neurogena, mielomeningocele, trauma con perdita funzionale irreversibile dello sfintere esterno), è preferibile confezionare una tasca eterotopica continente con stomia addominale a livello ombelicale. Il cateterismo intermittente trans-ombelicale di un reservoir tipo Mainz Pouch I risulta più semplice rispetto al cateterismo intermittente trans-uretrale, è legato ad un minor tasso di complicanze e permette di ottenere ottimi risultati cosmetici e di migliorare la qualità di vita rispetto alle forme di derivazione urinaria non continente (2). A questo proposito, il meccanismo di continenza, originariamente eseguito tramite una invaginazione ileo-ileale, viene attualmente eseguito utilizzando l’appendice vermiforme, sempre che essa sia presente e di morfologia adeguata (3). Per quanto riguarda il reimpianto ureterale, il tunnel sottomucoso rappresenta un’eccellente tecnica, in presenza di ureteri di calibro normale, con basso tasso di complicanze in termini di reflusso e di stenosi anastomotiche. In caso di ureteri dilatati con parete fibrotica esso risulta però gravato da una notevole percentuale di complicanze. In questi casi un’alternativa può essere rappresentata dalla tecnica di Abol-Enein, inizialmente sperimentata su un modello animale ed attualmente affermatasi con la pubblicazione di ottimi risultati clinici (4, 5). Tale tecnica, primariamente ideata per un reimpianto in neovescica ileale ortotopica (vedi capitolo 8.1 1 – Neovescica ileale con reimpianto ureterale in tunnel sieroso extra- murale), può essere utilizzata senza problemi anche quando si prevede il confezionamento di una derivazione urinaria continente tramite Mainz Pouch I.





















– Mobilizzazione del cieco, del colon destro e della flessura colica destra incidendo la doccia parietocolica destra e sezionando il legamento epato-colico ed eventualmente i legamenti gastro- e duodeno-colico e mobilizzazione del grande omento dal colon trasverso lungo il piano avascolare con apertura della borsa omentale. – Isolamento di 10-15 cm di cieco e colon ascendente e di 20-30 cm di ileo terminale (36- 45 cm di ileo terminale se si prevede di confezionare un’invaginazione ileale come meccanismo di continenza). – Ripristino della continuità intestinale tramite ileo-ascendostomia termino-terminale con punti staccati sieromuscolari in PDS. – Previa pulizia tramite lavaggio con fisiologica del segmento intestinale escluso dalla continuità intestinale apertura antimesenteriale (detubularizzazione) dello stesso. – Anastomosi latero-laterale dei vari segmenti intestinali esclusi: il colon con l’ansa ileale più distale e questa con il tratto ileale adiacente. Si viene così a creare il pavimento della tasca di Mainz. – Reimpianto ureterale nel segmento colico con tecnica open-end in un tunnel sottomucoso ed anastomosi uretero-intestinale muco-mucosa. – In presenza di un’appendice sufficientemente lunga e priva di processi flogistici si procede alla creazione di uno stoma appendicolare continente. A tale proposito si lasciano integri gli ultimi 4-5 cm di cieco in corso di apertura antimesenteriale. – Incisione dello strato sieromuscolare lungo la tenia antimesenterica a livello del polo cecale e fino alla base dell’appendice con creazione di un letto mucoso nel quale alloggiare l’appendice. – Il mesentere appendicolare viene liberato dal tessuto adiposo in eccesso, rispettandone la vascolarizzazione. – Si creano delle finestre attraverso il mesentere appendicolare. L’appendice viene aperta nel suo tratto distale, ripiegata su se stessa ed alloggiata nel letto sottomucoso. Il mesentere appendicolare rimane al di fuori del letto sottomucoso. – Chiusura dello strato sieromuscolare sopra l’appendice con punti staccati che passano attraverso le finestre mesenteriali precedentemente create. Si viene così a creare un meccanismo di continenza secondo il principio del flap-valve. – La porzione appendicolare distale aperta viene anastomizzata all’ombelico al termine dell’intervento. – In previsione di un’invaginazione ileo-ileale per il meccanismo di continenza è necessario isolare un segmento ileale ulteriore di ca. 12-16 cm. L’apertura antimesenteriale dell’intestino escluso risparmia il segmento ileale prossimale. La valvola ileo-cecale viene lasciata intatta. – Invaginazione ileo-ileale isoperistaltica di 6 cm dopo aver preparato e fenestrato il mesentere ileale, onde escludere quest’ultimo dall’invaginazione. – Cruentazione con cucchiaio di Volker della mucosa del nipple e del tunnel ileo-cecale. – L’invaginazione viene eseguita tramite 2 pinze di Allis attraverso il tunnel naturale costituito dalla valvola ileo-cecale e quindi fissata usando 2 file di punti metallici da 4,8 mm della suturatrice meccanica TA 55 alle ore 3 e 9. I primi quattro punti metallici della suturatrice meccanica vengono rimossi per evitare la futura formazione di calcoli. – Inoltre, l’invaginazione viene fissata alla parete della valvola ileo-cecale per mezzo di una fila di punti metallici (4,8 mm) fra le due pareti dell’invaginazione e la valvola ileo-cecale, inserendo la suturatrice TA 55 dall’interno del pouch nel tunnel ileocecale alle ore 12. – In alternativa, per diminuire il rischio dell’insorgenza di calcoli, è possibile fissare l’invaginazione alla parete posteriore della valvola ileo-cecale. In questo caso la suturatrice TA 55 viene inserita dall’esterno del pouch fino alla base dell’invaginazione. – Infine, la punta dell’invaginazione viene suturata all’apertura cecale della valvola con punti staccati in Dexon 4/0. – L’apertura ileale aborale dell’invaginazione viene anastomizzata all’ombelico al termine dell’intervento. – Chiusura della parete anteriore della tasca con materiale sintetico riassorbibile 4/0.
– Isolamento, preparazione e sezione dell’uretere destro. – Incisione paracolica sinistra, isolamento, sezione e spostamento retromesenteriale verso destra dell’uretere sinistro al di sopra dell’arteria mesenterica inferiore. – Isolamento del segmento intestinale preservando l’integrità dell’irrorazione: rispetto alla tecnica standard, esclusione dalla continuità intestinale di 24-30 cm di cieco e colon (2 x 12-15 cm) e di un solo segmento ileale di 12-15 cm. – Ripristino della continuità intestinale tramite anastomosi ileo-colica. – Previa pulizia tramite lavaggio con fisiologica del segmento intestinale escluso, incisione antimesenteriale dello stesso: rimane integro il solo polo cecale (per il meccanismo di continenza). – Formazione del meccanismo di continenza e posizionamento di un catetere nella tasca. – Riconfigurazione del segmento colico escluso in forma di V invertita. – Anastomosi colo-colica latero-laterale con sutura sieromuscolare in continua dei bracci mediali della V invertita con materiale non riassorbibile (ad es. Prolene 4/0). Si provvede a lasciare un’apertura all’estremità craniale della sutura per il successivo passaggio dell’uretere destro. Si è così formato un tunnel sieroso extra-murale ove alloggiare l’uretere destro. – Anastomosi latero-laterale dell’ansa ileale con il segmento colico adiacente attraverso identica sutura sieromuscolare in continua con materiale non riassorbibile. Si viene così a formare un secondo tunnel sieroso extra-murale ove verrà alloggiato l’uretere sinistro. – Incisione mesenteriale cranialmente alla sutura ileocolica ed alloggiamento dell’uretere sinistro nel corrispondente tunnel sieroso. – Spostamento dell’uretere destro attraverso l’apertura precedentemente lasciata all’estremità craniale della sutura colo-colica ad alloggiamento dello stesso nel corrispondente tunnel sieroso. – Anastomosi dei margini intestinali liberi al di sopra degli ureteri tramite sutura a tutto spessore in continua con materiale sintetico riassorbibile. Gli ureteri vengono così incorporati nella parete posteriore della tasca; la lunghezza del tunnel sieroso dovrebbe essere 4 volte superiore al diametro ureterale. – Anastomosi uretero-intestinale previa incisione longitudinale a becco di flauto ed accorciamento ureterale della lunghezza corrispondente. – Fissazione dell’ uretere tramite 4 punti a tutto spessore (intera parete ureterale ed intestinale) alle ore 11, 1, 5 e 7 (catgut cromico 4/0). – Adattamento muco-mucoso attraverso punti singoli (catgut cromico 5/0 o 6/0). – Splint ureterali (di spessore variabile in relazione alla dilatazione ureterale: Charr 6 – 12) e fissazione di questi con catgut 5/0 alla mucosa intestinale. – Previo posizionamento di una pouchostomia, sutura in continua della parete anteriore della tasca con materiale sintetico riassorbibile 4/0.
STENOSI DELLO STOMA – Occorrono quasi sempre a livello della fascia. – Possono essere risolte endoscopicamente in analogia alla tecnica dell’uretrotomia interna secondo Sachse procedendo ad eseguire un’incisione a forma di stella. – Stenosi a livello cutaneo sono più rare e necessitano di una plastica cutanea a Z. Tali stenosi possono essere prevenute eseguendo in sede di intervento primario un’anastomosi ombelicale a forma di V del segmento efferente (invaginazione ileo- ileale o appendice). SVAGINAMENTO DEL NIPPLE ILEO-ILEALE – Viene definito come dislocamento dell’invaginazione ileo-ileale al di fuori della valvola ileo-cecale. – Previa laparotomia mediana si procede ad aprire la parete laterale della tasca. – Si attrae l’invaginazione ileale all’interno della valvola ileo-cecale con due pinze di Allis. – Fissazione dell’invaginazione dall’interno con una fila di punti metallici da 4,8 mm della suturatrice meccanica TA 55. – Inoltre, fissazione con colla di fibrina e tramite sutura muco-mucosa tra nipple e valvola ileo-cecale. – Fissazione della tasca alla parete addominale anteriore. STENOSI DELL’IMPIANTO URETERALE – Stenosi asintomatiche o sintomatiche dell’impianto ureterale con un wash-out renale inferiore al 50 dopo somministrazione di furosemide necessitano di un reimpianto ureterale. – Paziente in decubito laterale sinistro. Accesso laterale sopracostale. Incisione cutanea tra punta della XII costa destra ed ombelico. Quest’accesso permette di ottenere un’esposizione ottimale dell’anastomosi uretero-intestinale. – Identificazione ed isolamento degli ureteri. – Apertura della tasca in parallelo al decorso ureterale. – Sezione dell’uretere stenotico a livello della sua dilatazione pre-stenotica all’ingresso nella tasca. – Legatura del moncone ureterale distale. – Reimpianto con tecnica “button-hole” previa incisione della parete posteriore della tasca. – Preparazione di un tunnel sottomucoso, che si viene a trovare tra i due tunnel originariamente preparati. Incisione longitudinale della mucosa colica. – Alloggiamento dell’uretere nel tunnel e riapprossimazione della mucosa colica al di sopra di esso. L’uretere viene fissato con 2 punti alle ore 5 e 7. – Splint ureterali in entrambi gli ureteri (anche quello non reimpiantato). Lo split dell’uretere reimpiantato viene rimosso in 14. giornata post-operatoria. L’altro può essere rimosso in 7. giornata. Drenaggio della tasca tramite stomia cutanea.
1. Thueroff JW, Alken P, Riedmiller H, Engelmann U, Jacobi GH, Hohenfellner R. The Mainz Pouch (Mixed Augmentation Ileum and Cecum) for bladder augmentation and continent diversion. J Urol 1986; 136: 17.2. Thueroff JW, Alken P, Riedmiller H, Jacobi GH, Hohenfellner R. 100 cases of Mainz Pouch: continuing experience and evolution. J Urol 1988; 140: 283.3. Riedmiller H, Burger R, Mueller SC, Thueroff JW, Hohenfellner R. Continent appendix stoma: a modification of the Mainz Pouch technique. J Urol 1990; 143: 115.4. Abol-Enein H, Ghoneim MA. Optimization of uretero-intestinal anastomosis in urinary diversion: an experimental study in dogs. III. A new antireflux technique for uretero-ileal anastomosis: a serous lined extramural tunnel. Urol Res 1993; 21: 135.5. Abol-Enein H, Ghoneim MA. A novel uretero-ileal reimplantation technique: the serous lined extramural tunnel. A preliminary report. J Urol 1995; 151: 1193.
Margit Fisch – Robert Wammack – Mohsen El-Mekresh – Rudolf Hohenfellner
Lesioni attiniche a lungo termine sono frequenti in pazienti sottoposti a radioterapia. In caso di radioterapia pelvica gli organi coinvolti nel campo di irradiazione comprendono gli ureteri distali e segmenti intestinali quali sigma, polo cecale ed ileo terminale. Se si pone indicazione ad una derivazione urinaria in questi pazienti è necessario utilizzare idealmente segmenti intestinali localizzati al di fuori del campo di irradiazione così come è necessario eseguire un reimpianto ureterale alto. Il colon trasverso risponde a questi requisiti: si trova al di fuori dei normali campi di irradiazione, consente una adeguata mobilizzazione in considerazione della lunghezza del suo mese e, vista la sua localizzazione craniale, permette un reimpianto ureterale alto dopo sezione della porzione distale degli ureteri. La decisione se confezionare un condotto colico-trasverso (vedi capitolo 8.5 – Condotto colico-trasverso) o una tasca colica continente dipende dalle condizioni generali e dall’aspettativa di vita del paziente. Punto fondamentale nella creazione di una tasca colica con il trasverso è rappresentato dal confezionamento di un efficace meccanismo di continenza. Inizialmente, il segmento efferente da abboccare alla cute (ombelico) era rappresentato da un breve ansa ileale esclusa, che veniva alloggiata in un letto mucoso dopo incisione sieromuscolare della parete colica. La più recente modificazione prevede di utilizzare come ansa efferente un segmento colico assottigliato ripiegato su se stesso e alloggiato in un letto mucoso nella parete stessa della tasca creando così il meccanismo di continenza utilizzando lo stesso segmento colico utilizzato per formare la tasca. Tale modificazione presenta l’innegabile vantaggio di consentire il risparmio di un segmento ileale supplementare con conseguente rinuncia ad una seconda anastomosi intestinale.




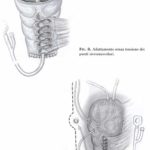


– Derivazione urinaria in presenza di neoplasia maligna pelvica urologica, ginecologica o intestinale precedentemente sottoposta a radioterapia o in cui si preveda di eseguire una radioterapia adiuvante. – Incontinenza a seguito di cistite attinica. – Fistole vescico-vaginali o vescico-vagino-intestinali dopo radioterapia pelvica.
– In corso di laparotomia mediana si procede ad una incisione latero-ombelicale destra in quanto la tasca colico-trasversa si verrà a trovare nell’emiaddome sinistro e la conseguente anastomosi del segmento efferente con l’ombelico risulterà in questo caso più semplice. Se si prevede di utilizzare un segmento di colon ascendente per la tasca colica allora si procede con la classica incisione latero-ombelicale sinistra in quanto il reservoir si verrà a trovare nell’emiaddome destro. – Esclusione del colon trasverso ed eventualmente di una parte del colon ascendente o discendente dalla continuità intestinale per una lunghezza totale di ca. 30-34 cm. – Ripristino della continuità intestinale con anastomosi termine-terminale colo-colica con sutura a punti staccati sieromuscolare in PDS 4/0. – Chiusura della finestra mesenteriale previamente incisa in corso di esclusione del segmento intestinale. – Lavaggio del segmento intestinale escluso. – Chiusura dell’estremità orale del segmento intestinale escluso. – Riconfigurazione del segmento intestinale escluso in forma di V invertita con il braccio destro (orale) della V più lungo di ca. 10 cm. – Apertura del segmento intestinale lungo la tenia libera lasciando integri gli ultimi 10 cm dell’estremità orale. – Anastomosi latero-laterale delle anse intestinali mediali approssimate. – Reimpianto ureterale in un tunnel sottomucoso. – Esclusione dalla continuità intestinale di un segmento ileale di ca. 10 cm che verrà poi utilizzato come segmento efferente per la creazione del meccanismo di continenza ed abboccato all’ombelico. – Ripristino della continuità intestinale con anastomosi tcrmino-terminale ileo-ileale con sutura sieromuscolare a punti staccati in PDS 4/0. – Lavaggio del segmento ileale escluso. – Posizionamento di un catetere 18 Charr nel segmento ileale inserendolo dall’estremità aborale. – Assottigliamento del segmento ileale sulla guida del catetere e sutura antimesenteriale emostatica in continua a doppio strato con materiale non riassorbibile. – Preparazione delle finestre mesenteriali. – Incisione sieromuscolare lungo la tenia libera del segmento colico non detubularizzato e lasciato intatto a partire dall’estremità orale precedentemente chiusa. – Preparazione del letto mucoso sottominando la sieromuscolare ai due lati dell’incisione. – Incisione trasversale di 1 cm della mucosa colica all’estremità craniale del letto mucoso preformato. – Anastomosi dell’estremità orale del segmento ileale con l’apertura mucosa colica a livello del letto mucoso, previo inserimento del catetere lungo la stessa incisione mucosa nella tasca colica. – Posizionamento dei punti sieromuscolari attraverso le finestre mesenteriali. – Adattamento con legatura senza tensione dei punti sieromuscolari precedentemente posizionati sul segmento ileale alloggiato nel letto mucoso colico per creare il meccanismo di continenza. – Fissazione dell’estremità aborale del segmento ileale efferente alla sieromuscolare colica. – Chiusura della parete anteriore della tasca. – Formazione dello stoma ombelicale.
– Previa esclusione del segmento colico si procede alla sua riconfigurazione a forma di U invertita lasciando l’estremità orale più lunga di ca. 5 cm. – Posizionamento di un catetere Charr 20 inserendolo dall’estremità orale. – Assottigliamento dell’estremità orale resecando una semiluna di parete colica di 5 cm di lunghezza e 2 cm di larghezza sulla guida del catetere precedentemente posizionato. – Chiusura in doppio strato del segmento colico assottigliato sulla guida del catetere (mucosa in Monocryl 4/0, sieromuscolare in PDS 4/0). – Preparazione di finestre mesenteriali a livello del segmento assottigliato. – Apertura con conseguente detubularizzazione del restante segmento colico escluso dalla continuità intestinale. – Anastomosi latero-laterale con sutura in continua dei margini mediali approssimati. – Reimpianto ureterale in tunnel sottomucoso. – Chiusura della parete anteriore della tasca. – Ripiegamento su se stesso del segmento assottigliato per la creazione del futuro meccanismo di continenza. – Tale segmento viene alloggiato sulla parete esterna della tasca lungo la sutura della sua parete anteriore. – Adattamento con legatura senza tensione della parete sieromuscolare della tasca sul segmento assottigliato con punti staccati fatti passare attraverso le finestre mesenteriali. In questo modo si incorpora il segmento efferente nella parete della tasca e si crea il meccanismo di continenza secondo il principio del flap-valve. – Formazione dello stoma ombelicale.
1. Hohenfellner R, Wulff HD. Zur Harnableitung mittels ausgeschalteter Darmsegmente. Akt Urol 1970; 1: 18.2. Duckett JW, Snyder HM. Continent urinary diversion: variations of Mitrofanoff principle. J Urol 1986; 136: 58.3. Eshgi M, Bronsther B, Ansong K, Hanna MK, Smith DD. Technique and trial of continent ileocystostomy. Urology 1986; 27: 112.4. Lampel A, Hohenfellner M, SchuItz-Lampel D, Thueroff JW. In situ tunnelled bowel flap tubes: 2 new techniques of a continent outlet for Mainz Pouch cutaneous diversion. J Urol 1995; 153: 308.
Vincenzo Disanto – Massimo Barile
Seguendo la classificazione della “International Continence Society” le derivazioni urinarie continenti si dividono in derivazioni trans-sfinteriche, trans-anali e trans- stoma addominale. Tra queste varie alternative quella certamente più gradita al paziente e, allo stesso tempo, gratificante per il chirurgo è la derivazione continente trans-sfinterica o sostituzione ortotopica di vescica. Questa soluzione è quella che più rispetta l’integrità fisica del paziente consentendo, al tempo stesso, il mantenimento della minzione “per uretram”. Tra le varie soluzioni tecniche a disposizione abbiamo dato la preferenza, dal 1989, alla neovescica sigmoidea perché questa, oltre a fornirci la protezione ottimale dell’apparato urinario alto, una buona capacità ed una buona compliance, presenta delle caratteristiche che la differenziano dalle neovesciche ileali. Infatti, la neovescica ortotopica sigmoidea detubularizzata permette al paziente di avvertire la sensazione di riempimento vescicale e, soprattutto, mantiene nel tempo le sue caratteristiche morfologiche e funzionali. Al fine di definire l’indicazione ad una neovescica ortotopica sigmoidea, oltre alla comune diagnostica, sono necessari i seguenti esami: 1) Biopsie multiple dell’uretra prostatica, alle ore 3-6-9-12 ed in sede pericollicolare. Prelievi “a freddo” vengono eseguiti inoltre nell’uretra bulbare, nell’uretra anteriore ed in tutte le aree sospette. 2) Esame urodinamico: profilo pressorio uretrale e stop test al fine di valutare il buon funzionamento dello sfintere striato. 3) Clisma opaco e colonscopia sono due esami di routine quando ci si accinga a realizzare una neovescica sigmoidea.



– Completata la cistoprostatovesciculectomia e la linfadenectomia pelvica avendo cura di rispettare il moncone prossimale dell’uretra membranosa, si procede all’isolamento del sigma che viene liberato da tutte le briglie peritoneali che in qualche modo potrebbero ostacolarne la discesa nel piccolo bacino. – Il sigma, ripiegato ad U, deve poter discendere agevolmente fino al piano perineale. Talora può essere difficile portare l’estremità distale della L a contatto dell’uretra a causa di una arteria mesenterica inferiore di lunghezza insufficiente. In questi casi è possibile sezionare senza conseguenze uno dei rami sigmoidei per portare senza problemi il viscere al piano perineale. – Non si può tuttavia escludere l’eventualità di un sigma non utilizzabile per la sostituzione. In questi casi è preferibile, piuttosto che realizzare una anastomosi sotto tensione, rinunciare alla costruzione di una neovescica sigmoidea ed utilizzare l’ileo, oppure scegliere un altro tipo di derivazione urinaria. – L’ansa sigmoidea deve avere una lunghezza non inferiore ai 25-30 cm e, rispettandone la vascolarizzazione, viene sezionata tra due enterostati. – Si procede quindi alla ricostruzione della continuità intestinale con un’anastomosi termino-terminale a punti staccati in doppio strato in Dexon 3/0. – Dopo essere stata lavata con una soluzione antibiotica, l’ansa sigmoidea viene configurata ad U ed adagiata nello scavo pelvico. – Nell’eseguire questa manovra l’ansa viene fatta ruotare di 180° sul suo asse portando a destra il moncone più prossimale ed a sinistra il moncone distale. Così facendo è possibile evitare di sezionare il ramo terminale dell’arteria mesenterica inferiore garantendo la vascolarizzazione del retto e della anastomosi colo-colica. La rotazione di 180° dell’arteria mesenterica inferiore sul suo asse non riduce il flusso arterioso. – Si procede quindi all’apertura dell’ansa lungo la tenia anteriore. – I margini posteriori della sezione longitudinale dell’ansa vengono suturati in doppio strato muco-mucoso e siero-muscolare utilizzando delle continue in Dexon 3/0. – Costruito così il piatto posteriore si procede all’anastomosi degli ureteri. Questi vengono fatti passare attraverso un tunnel sottomucoso lungo circa 3 cm. – Due stents ureterici (Charr 7-8) vengono fatti fuoriuscire controlateralmente attraverso la parete della neovescica. – Nella parte inferiore della tasca viene praticata un’apertura, sufficientemente ampia da permettere una agevole anastomosi all’uretra con 6 punti in Dexon 3/0. Viene lasciato un catetere uretrale di Foley 22 Charr. – Il confezionamento della neovescica si conclude con la sutura del margine longitudinale anteriore e dell’estremità craniale. La sutura in Dexon 3/0 viene realizzata con delle continue in doppio strato. – Ogni volta che sia possibile è opportuno procedere alla ricostruzione del sacco peritoneale. – Normalmente non vi è necessità di drenare la neovescica attraverso una sonda sovrapubica. – Due drenaggi vengono posizionati nello scavo pelvico.
– L’alimentazione parenterale viene utilizzata per circa 8 giorni, assicurando un apporto calorico sufficiente. – Il paziente viene mobilizzato in 3. giornata. – I drenaggi vengono rimossi appena si riduce la secrezione linfatica, in genere dopo 5-6 giorni. – I tutori ureterali vengono rimossi in 10. giornata. – E’ necessario garantire la pervietà del catetere uretrale con lavaggi vescicali con soluzione fisiologica che nei primi 4-5 giorni vengono effettuati ogni 4 ore e successivamente ogni 12 ore. – Indispensabile la terapia antibiotica e la profilassi antitrombotica con eparina a basso dosaggio. – Il paziente viene dimesso in 10. giornata, con il catetere, e la prescrizione di lavaggi della tasca, con soluzione fisiologica sterile, una volta al giorno. – In 28. giornata il paziente viene sottoposto a cistografia seguita dalla rimozione del catetere.
1. Reddy PK. Detubularized sigmoid reservoir for bladder replacement after cystoprostatectomy. Urology 1987; 29: 625.2. Wenderoth UV, Bachor B, Egghast G, Frohneberg D, Miller K, Hautmann RE. The ileal neobladder: experience and results of more than 100 consecutive cases. J Urol 1990; 143: 492.3. Pagano F, Artibani W, Ligato P, Piazza R. Gabeglio A, Passerini G. Vescica ileale padovana: a technique for total bladder remplacement. Eur Urol 1990; 17: 149.4. Chen K, Change LS, Chen MT. Neobladder construction using completely detubularized sigmoid colon after radical cystoprostatectomy. J Urol 1991; 146: 311.5. Disanto V, Barile M, Dituro A, Azzone D, Ventura F, Romano M, Portoghese F, Martalo S. La neovescica ortotopica con ansa sigmoidea detubulizzata. Acta Urol 1991; 6(suppl. I): 615.6. Reddy PK, Lange PH, Fraley EE. Total bladder remplacement using detubularized sigmoid colon: technique and results. J Urol 1991; 145: 51.7. Pompa P, Di Girolamo V, Colombo R, Bertini R, Canovaro G, Da Pozzo L, Rigatti P. Valutazione dello squilibrio elettrolitico ed acido-base in paziente con neovescica sigmoidea ortotopica. Acta Urol Ital 1992; suppl. 4: 151.8. Disanto V, Martalo S, Portoghese F. Qualità di vita in pazienti affetti da carcinoma infiltrante della vescica in fase avanzata sottoposti a derivazione ortotopica sigmoidea dopo cistoprostatovesciculectomia. Acta Urol Ital 1992; suppl. 4: 149.9. Pompa P, Colombo R, Da Pozzo L, Scattoni V, Digirolamo V, Berlini R, Rigatti P. Neovescica ortotopica sigmoidea di sostituzione. Valutazione clinica ed urodinamica in follow-up a lungo termine. Acta Urol Ital 1993; suppl. 2: 163.10. Martalo S, Portoghese F, Disanto V. Valutazione del metabolismo elettrolitico ed acido-base in 16 pazienti sottoposti a cistectomia radicale e derivazione ortotopica con ansa sigmoidea detubulizzata. Acta Urol Ital 1993; suppl. 2: 117.11. Da Pozzo LE, Colombo R, Pompa P, Montorsi F, Di Girolamo V, Rigatti P. Detubularized sigmoid colon for bladder replacement after radical cystectomy. J Urol 1994; 152: 1409.
Urs E. Studer – Hansjoerg Danuser – Ernst J. Zingg
La neovescica ileale ortotopica e oggi una forma di derivazione urinaria di uso comune. Una accurata selezione dei pazienti unitamente ad una tecnica chirurgica precisa, al training minzionale con il torchio addominale e ad un accurato follow-np rappresentano parametri fondamentali per ottenere dei linoni risultati a distanza. La procedura qui di seguito descritta non presenta difficoltà tecniche superiori rispetto al confezionamento di un condotto ileale. Il segmento ileale utilizzato è lungo circa il triplo rispetto al segmento intestinale utilizzato per un condotto ileale. La sua estremità aborale viene detubularizzata a formare un serbatoio urinario a bassa pressione secondo il principio della “cup-patch-technique” di Goodwin e viene anastomizzata all’uretra membranosa (1). Al fine di evitare sindromi di malassorbimento intestinale si lasciano integri sia l’ileo terminale sia la valvola ileo-cecale. Il serbatoio viene creato con soli 40-44 cm di ileo. In questo modo si ottiene uno svuotamento vescicale completo senza residuo post-minzionale. La superficie intestinale assorbente ed il tempo in cui l’urina è a contatto con la mucosa intestinale risultano ridotte rispetto ad altre forme di neovesciche più ampie. La capacità del serbatoio (ca. 500 ml) consente tuttavia di ottenere basse pressioni sufficienti a garantire la continenza urinaria. In questo modo si evita anche la formazione di un serbatoio troppo ampio e flaccido incapace di svuotarsi completamente (2). L’uso di un segmento ileale afferente, isoperistaltico e non-detubularizzato consente la sezione alta degli ureteri con rimozione in blocco del preparato vescica-ureteri distali. Ciò riduce il rischio di recidive tumorali ureterali a livello dell’uretere distale. La peristalsi del segmento ileale afferente associata alla citata bassa pressione del serbatoio consente di ottenere un meccanismo dinamico antireflusso sufficiente e di evitare un reimpianto ureterale antireflusso con il suo rischio intrinseco di complicanze (3). Inoltre, la sezione ureterale al di sopra dei vasi ilaci permette di minimizzare il rischio di una ischemia ureterale distale spesso associata a complicanze stenotiche. Nel raro caso di una ostruzione funzionale allo svuotamento vescicale, di una recidiva locale sintomatica a livello pelvico o della necessità di una uretrectomia secondaria, è possibile convertire senza problemi la neovescica ileale in un condotto ileale. Pre-requisiti fondamentali per il confezionamento di una neovescica ortotopica ileale sono rappresentati da una buona funzionalità renale con creatinina sierica < 2 mg/dl, dall’assenza di metastasi a distanza, dall’assenza di tumore a livello della biopsia prostatica collicolare e dalla buona compliance del paziente.




RESEZIONE INTESTINALE – Esclusione dalla continuità intestinale di un segmento ileale di ca. 54-60 cm ad una distanza di 25 cm dalla valvola ileo-cecale. In presenza di un catetere peridurale a infusione continua di anestetico locale è possibile una notevole retrazione intestinale così che dopo rilassamento il segmento escluso potrebbe risultare troppo lungo. – L’incisione distale del mesentere, lunga ca. 15-20 cm, preserva l’arteria ileo-cecale, mentre l’incisione prossimale, lunga ca. 5-8 cm, preserva almeno due arcate vascolari per l’adeguata vascolarizzazione del segmento intestinale escluso. – Ripristino della continuità intestinale con anastomosi ileo-ileale termino-terminale in Vicryl 4/0 in sutura sieromuscolare continua. – Chiusura dell’incisione mesenteriale con sutura in continua in Vicryl 2/0. – Le due estremità del segmento ileale escluso vengono chiuse con sutura in continua sieromuscolare in Vicryl 4/0. – I 40-44 cm distali del segmento ileale escluso vengono aperti sul bordo antimesenterico con le forbici lasciando i restanti 14-16 cm prossimali integri. REIMPIANTO URETERALE – Previo spostamento dell’uretere sinistro verso l’area paracavale destra, passando al di sopra dell’origine dell’arteria mesenterica inferiore, si procede all’incisione a becco di flauto di entrambi gli ureteri per una lunghezza di ca. 1,5 cm. – Incisione longitudinale di ca. 2 cm a livello dell’estremità prossimale del segmento ileale afferente integro non-detubularizzato lungo il margine antimesenteriale in zona paramediana. L’incisione per il reimpianto dell’uretere destro avviene ca. 1 cm più in basso rispetto a quella fatta per l’uretere sinistro. – Anastomosi uretero-intestinale sieromuscolare in continua in Vicryl 4/0. E’ necessario passare il punto prima a livello della parete ureterale, in modo che questa si venga a trovare sempre tra mucosa e sieromuscolare ileale. Ciò consente una sutura impermeabile ed evita il prolasso di mucosa ileale e la retrazione della anastomosi. – Prima del termine del reimpianto si procede a posizionare i tutori ureterali che vendono poi fatti passare attraverso il segmento ileale afferente e portati verso il basso raggiungendo la futura neoveseica ileale. I tutori ureterali vengono fissati con Vicryl rapid e fatti fuoriuscire dal lume a livello dell’estremità distale del segmento ileale afferente. CREAZIONE DELLA NEOVESCICA – Riconfigurazione a U del segmento ileale detubularizzato e susseguente sutura latero- laterale dei margini mediali approssimati in Vicryl 2/0. – Ripiegamento su se stesso della punta della U in modo da formare un serbatoio di grossa capacità a partire da 4 segmenti ileali aperti. – Chiusura della porzione più caudale e dei 2/3 craniali della parete anteriore del serbatoio con sutura sieromuscolare in continua in Vicryl 2/0. – Previo inserimento del dito indice nel serbatoio attraverso l’apertura lasciata in precedenza si procede ad identificare il punto più declive del reservoir a ca. 1,5 cm di distanza dalla sutura ili continua caudale della parete anteriore ed a ca. 3 cm di distanza dal termine della sutura citata. In questa maniera si evita la formazione di una anastomosi imbutiforme che potrebbe risolvere in ripiegamenti ed incompleto svuotamento vescicale in corso di torchio addominale. – Si forma a questo livello un foro di ca. 8-10 inni di diametro con le forbici. – Si passano 6 punti anastomotici in Vicryl 6/0 tra l’incisione al punto più declive del serbatoio e l’uretra membranosa. Sul lato ileale i punti sono sieromuscolari. Sul lato uretrale, i punti esterni vengono passati a ca. 4 mm di distanza dal margine di resezione mentre quelli interni a livello del bordo mucoso. In tal modo si ottiene un ottimale adattamento muco-mucoso. – I due punti più dorsali includono anche la membrana del Denonvillier mentre quelli più ventrali includono i lembi del plesso del Santorini legato in sede di cistectomia. In questo modo si ottiene una eguale trazione su tutti i lati dell’anastomosi evitando lesioni dell’apparato sfinterico. – Previo inserimento di un catetere 18 Charr si legano i punti anastomotici così posizionati, a partire dai punti ventrali (ore 11 e 13), proseguendo con quelli alle ore 9 e 3 ed alle ore 7 e 5. – Posizionamento di una epicistostomia. – Si completa la chiusura della neovescica.
– Lavaggio della neovescica ogni 6 ore con 50 ml di soluzione fisiologica attraverso il catetere vescicale e l’epicistostomia. – Controllo dell’equilibrio acido-base e degli elettroliti sierici ogni 2 giorni fino a quando l’eventuale acidosi non si sia stabilizzata. In presenza di un eccesso basi inferiore a – 2 mmol/1 si procede alla somministrazione di 2-4 g di bicarbonato di sodio. – Rimozione ilei tutori ureterali in 6.-7. giornata post-operatoria. – Cistografia in 9.-10. giornata post-operatoria. In assenza di stravaso, rimozione dell’epicistostomia. – Rimozione del catetere vescicale in 12. giornata post-operatoria. – Dopo la rimozione del catetere inizia la ginnastica vescicale con minzione seduta sotto moderato torchio addominale ogni 2 ore (ogni 3 ore durante la notte) e contemporaneo rilassamento dell’apparato sfinterico. – Nei primi giorni dopo il ripristino della minzione spontanea si controlla il residuo post-minzionale tramite ecografia. – Costante prolungamento dell’intervallo tra le minzioni fino a 3-4 ore. Anche in presenza di una incontinenza e necessario che il paziente tenti di prolungare l’intervallo tra le minzioni. Solo in questa maniera sarà possibile creare delle pressioni endoluminali maggiori e di conseguenza aumentare la capacità della neovescica. I pericoli di una minzione troppo frequente sono quelli di una ridotta capacità neovescicale a lungo termine con conseguenti permanenti elevate pressioni endoluminali ed incontinenza permanente. – A questo proposito è necessaria l’accurata informazione del paziente: il raggiungimento di una pressione endovescicale bassa e quindi della continenza urinaria sarà ottenibile solo quando la capacità della neovescica abbia raggiunto i 400-500 ml. Una semplice analogia da proporre al paziente è rappresentata dal gonfiare un palloncino: quando il palloncino è sgonfio e piccolo è necessaria una elevata pressione per gonfiarlo; man mano che il diametro del palloncino aumenta, diminuisce anche la pressione necessaria a gonfiarlo. – L’incontinenza temporanea è il prezzo da pagare per raggiungere una adeguata capacità vescicale prolungando gli intervalli tra le minzioni. Altrimenti, si corre il rischio di una incontinenza permanente, specie notturna. – Dato che viene a mancare il riflesso minzionale è necessario svegliarsi la notte inizialmente almeno 2 volte per svuotare la neovescica ogni 3 ore. Ad un anno di distanza dall’intervento è possibile svuotare la vescica durante la notte ogni 4-5 ore. – Seguendo adeguate istruzioni ed a 3 mesi di distanza dall’intervento, il paziente con neovescica ileale dovrebbe raggiungere idealmente un intervallo tra le minzioni di ca. 4 ore, una capacità vescicale di 400-500 ml ed ottenere uno svuotamento vescicale completo in assenza di residuo.
1. Goodwin WE, Winter CC, Barker WF. “Cup-patch” technique of ileocystoplasty for bladder enlargement or partial substitution. Surg Gynecol Obstet 1959; 108: 240.2. Studer UE, Danuser H, Merz VW, Springer JP, Zingg EJ. Experience in 100 patients with an ileal low pressure bladder substitute combined with an afferent tubular isoperistaltic segment. J Urol 1995; 154: 49.3. Studer UE, Danuser H, Thalmann GN, Springer JP, Turner WH. Antireflux nipples or afferent tubular segments in 70 patients with ileal low pressure bladder substitutes: long term results of a prospective randomized trial. J Urol 1996; 156: 1913.
Francesco Pagano – Walter Artibani – Giacomo Passerini-Glazel – Pierfrancesco Bassi
La vescica ileale padovana (VIP) rappresenta una procedura chirurgica semplice e veloce per la formazione di un reservoir ortotopico detubularizzato e riconfìgurato di aspetto sferico simile alla vescica originale (1). A causa delle complicanze recentemente pubblicate (2, 3) la tecnica di reimpianto ureterale secondo Le Duc (4) è stata sostituita dal reimpianto in tunnel sieroso extra-murale secondo Abol-Enein (5).





– L’ultimo passaggio della cistectomla radicale è rappresentato dalla sezione dell’uretra membranosa il più vicino possibile all’apice prostatico, in analogia alla tecnica della prostatectomia radicale. – Isolamento di un segmento ileale di 40-60 cm, la cui estremità aborale si trova ad una distanza di ca. 15-20 cm dalla valvola ileocecale. – Ripristino della continuità intestinale tramite anastomosi termino-terminale ileo- ileale. – Il segmento ileale viene aperto lungo il margine antimesenterico. – Inferiormente viene creato un imbuto mediante 2 suture continue, una posteriore ed una anteriore per ca. 5 cm, al fine di consentire una anastomosi uretro-ileale semplice e priva di tensione. – Ripiegamento a forma di L) rovesciata dell’ansa prossimale in senso mediale con anastomosi latore-laterale dei margini intestinali interni adiacenti. Si viene così a formare la parete posteriore e la cupola della neovescica. – I restanti margini intestinali affrontati vengono suturati latero-lateralmente. Si viene così a creare un reservoir sferico-ovoidale. – Reimpianto ureterale secondo la tecnica di Le Duc. Gli ureteri vengono drenati con tutori ureterali 6-8 Charr. – Anastomosi uretro-ileale al punto più declive della neovescica con 6 punti staccati in catgut cromico. In caso di mesentere troppo breve con limitata mobilità della neovescica è possibile eseguire l’anastomosi al limite inferiore della sutura anteriore dell’imbuto. Si guadagna così un tratto di ca. 2 cm di lunghezza. – Chiusura della parete anteriore della neovescica tramite sutura del margine della cupola con il margine inferiore. – Catetere vescicale trans-uretrale 22 Charr.
– Rimozione dei tutori ureterali in 7.-8. giornata post-operatoria. – Cistografia a 2-3 settimane di distanza dall’intervento: se non si riscontrano stravasi si rimuove il catetere vescicale. – Orografia endovenosa e videourodinamica a 3, 6 e 12 settimane di distanza dall’intervento. – Uretrocistoscopia annuale. – Training, eventualmente sotto controllo videourodinamico, per lo svuotamento della vescica sotto torchio addominale con contemporaneo rilasciamento del pavimento pelvico.
– Dopo detubularizzazione e riconfigurazione si anastomizzano i margini ileali approssimati con sutura siero-muscolare per creare due tunnel sierosi ove alloggiare gli ureteri. – Dopo aver alloggiato gli ureteri nei corrispondenti tunnel si procede all’anastomosi muco-mucosa tra uretere e intestino. – Infine si suturano i margini in eccesso della parete ileale al di sopra degli ureteri.
1. Pagano F, Artibani W, Ligato P, Piazza R, Garbeglio A, Passerini G. Vescica ileale padovana (VIP): a technique for total bladder replacement. Eur Urol 1990: 17: 149.2. Pagano F, Artibani W, Bassi P, Ruffato A, Mulonia A, Maio A. The paduan ileal bladder (V.I.R). Acta Urol Ital 1996; 10: 79.3. Roth S, van Ahlen H, Semjonow A, Oberpenning F, Hertle L. Does the success of uretero-intestinal implantation in orthotopic bladder substitution depend more on surgeon level of experience or choice of technique? J Urol 1997; 157: 56.4. Le Duc A, Camey M, Teillac P. An original antireflux uretero-ileal implantation technique: long term follow up. J Urol 1987; 137: 1156.5. Abol-Enein H, Ghoneim MA. A novel uretero-ileal reimplantation technique: the serous lined extramural tunnel. A preliminary report. J Urol 1994; 151: 1193.
Hassan Abol-Enein – Mohamed A. Ghoneim
Una tecnica ideale per il reimpianto ureterale in corso di derivazione urinaria continente dovrebbe comprendere i seguenti pre-requisiti: 1) Semplicità tecnica e riproducibilità clinica. 2) Flusso urinario unidirezionale antireflusso in assenza di stenosi anastomotiche a lungo termine. 3) Evitare l’uso di suturatrici meccaniche o materiale sintetico come anche l’utilizzo di un segmento intestinale eccessivamente lungo. 4) Possibilità di eseguire successivamente esami endoscopici retrogradi del tratto urinario alto, manovra peraltro facilitata dall’eventuale decorso ureterale rettilineo. 5) Versatilità, cioè tecnica applicabile indipendentemente dal calibro dell’uretere. Il nipple invaginato (1) e l’ansa ileale afferente (2) mancano di molti di questi criteri. La tecnica di Le Duc (3) è gravata da un elevato tasso di complicanze a causa di un difetto di rigenerazione degli ureteri reimpiantati con conseguenti stenosi e/o reflusso (4, 5). La tecnica qui proposta, ideata originariamente per il reimpianto ureterale in neovescica ileale ma applicabile con successo anche in altre forme di derivazione urinaria (vedi capitolo 8.2 – Tasca retto-sigmoidea – e capitolo 8.6 – Tasca ileo-cecale), risponde invece a tutti i pre-requisiti citati presentando ottimi risultati a lungo termine (6, 7).



– Completata la linfadenectomia e la sezione distale degli ureteri, gli ultimi tempi della cistectomia devono essere eseguiti accuratamente ponendo attenzione a non danneggiare il moncone uretrale e la muscolatura periuretrale. – Isolamento di un segmento di ileo distale della lunghezza di 40 cm e riconfigurazione di esso a W tramite il posizionamento di punti di ancoraggio. – Il versante antimesenterico dell’intestino è inciso con elettrobisturi. – I margini dei due lembi mediali sono anastomizzati tramite sutura a tutto spessore in continua (poliglactina 3/0). – Le estremità laterali della W sono approssimate al segmento mediale e suturate tra di loro con una sutura sieromuscolare in continua (seta 3/0). Si ottiene così la formazione di due tunnel sierosi, la cui parete posteriore è formata dalla sutura in continua in seta. – Chiusura della parete anteriore della neovescica nella sua porzione inferiore. – A livello del punto più caudale si crea un foro di 2 cm di diametro preferibilmente facendo saltare i punti dell’anastomosi mediana per una lunghezza di 2 cm. – Anastomosi del moncone uretrale (nel quale è stato introdotto un catetere in silicone 20 Charr) con il foro precedentemente formato utilizzando i punti di ancoraggio in poliglactina 4/0 precedentemente posizionati. – Mobilizzazione dell’uretere sinistro verso destra attraverso una finestra mesenteriale ottenuta a livello del mesocolon sinistro. Durante questa manovra è importante evitare angolazioni dell’uretere. – Alloggiamento degli ureteri nei rispettivi tunnel sierosi. – Anastomosi muco-mucosa degli ureteri con la mucosa intestinale all’estremità distale del tunneL Un tunnel di 2 cm di lunghezza è sufficiente in presenza di ureteri di normale calibro. – Anastomosi del margine mucoso del tunnel al di sopra dell’uretere con punti singoli o con sutura in continua a punti staccati (poliglactina 4/0). Fissazione degli ureteri al loro ingresso nel tunnel tramite un punto comprendente la sola avventizia. – Posizionamento di due stent (catetere di Websinger di calibro corrispondente all’uretere) e fissazione degli stessi alla parete intestinale con catgut 4/0. – Chiusura della neovescica con sutura in continua in singolo strato (poliglactina 3/0).
– Una leggera corrente diatermica della sutura sieromuscolare alla base dei tunnel sierosi induce aderenze che rinforzano le linee di sutura. – L’eversione della mucosa ileale a livello dell’apertura della neovescica assicura un adeguato adattamento dell’anastomosi uretro-ileale. – I punti di ancoraggio (poliglactina 4/0) alle ore 3, 9 e 12 devono includere la mucosa ed il tessuto muscolare peri-uretrale al fine di evitare la retrazione del moncone uretrale.
– Nutrizione parenterale fino alla ricomparsa di una normale funzione intestinale. – Terapia antibiotica per 5-7 giorni. – Rimozione degli stenta ureterali in 10.-11. giornata. – Lavaggio della neovescica attraverso il catetere trans-uretrale a partire dalla 7. giornata. – Prima della rimozione del catetere trans-uretrale (3. settimana post-operatoria), controllo radiologico (contrastografia, urografìa) della tenuta dell’anastomosi.
1. Kock NG, Nilson AE, Norlen L, Sundin T, Trasti H. Urinary diversion via a continent ileum reservoir: clinical experience. Scand J Urol Nephrol 1982; 49 (Suppl): 23.2. Studer UE, Gerber E, Springer J, Zingg EJ. Bladder reconstruction with bowel after radical cystectomy. World J Urol 1992; 10: 11.3. Le Duc A, Camey M, Teillac P. An original antireflux ureteroileal implantation technique: long term follow-up. J Urol 1987; 137: 1156.4. Abol-Enein H, El-Baz M, Ghoneim MA. Optimization of uretero-intestinal anastomosis in urinary diversion: an experimental study in dogs. 1. Evaluation of the Le Duc technique. Urol Res 1993; 21: 125.5. Abol-Enein H, El-Baz M, Ghoneim MA. Optimization of uretero-intestinal anastomosis in urinary diversion: an experimental study in dogs. II. Influence of exposure to urine on the healing of the ureter and ileum. Urol Res 1993; 21: 131.6. Abol-Enein H, Ghoneim MA. Optimization of uretero-intestinal anastomosis in urinary diversion: an experimental study in dogs. III. A new antireflux technique for uretero-ileal anastomosis: a serous lined extramural tunnel. Urol Res 1993; 21: 135.7. Abol-Enein H, Ghoneim MA. A novel uretero-ileal reimplantation technique: the serous lined extramural tunnel. A preliminary report. J Urol 1995; 151: 1193.